火石研究院盘点 进入特别审批与优先审批程序的基因检测体外诊断产品
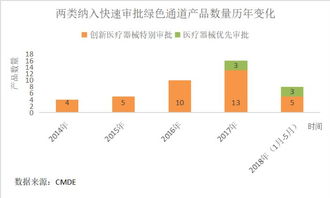
随着精准医疗和基因科技的快速发展,体外诊断(IVD)产品,特别是基因检测相关产品,在疾病预防、诊断和治疗中扮演着越来越关键的角色。为加速创新产品的上市进程,我国药品监督管理部门设立了特别审批程序和优先审批程序,旨在为具有显著临床价值的医疗器械提供快速通道。火石研究院对近年来纳入这两大审批程序的基因检测类体外诊断产品进行了系统性盘点,以洞察行业创新趋势与监管支持重点。
一、审批程序概述:加速创新产品临床转化
特别审批程序主要针对用于应对重大公共卫生事件或临床急需的医疗器械,在突发公共卫生事件应急等特殊情况下启动,强调“早期介入、随报随审”。而优先审批程序则面向具有明显临床优势,如诊断或治疗罕见病、恶性肿瘤,且具有显著临床价值的医疗器械,实行“优先审评、优先核查”,以缩短其上市周期。这两大程序为基因检测等高科技IVD产品从研发走向市场提供了重要助力。
二、重点产品盘点:聚焦肿瘤与感染性疾病领域
根据公开信息梳理,纳入特别审批和优先审批程序的基因检测IVD产品主要集中在以下几个方向:
- 肿瘤伴随诊断与早筛:
- 多基因联检试剂盒:多个基于高通量测序(NGS)技术的肿瘤基因突变检测试剂盒,用于非小细胞肺癌、结直肠癌等实体瘤的伴随诊断,指导靶向用药,已通过优先审批通道获批上市。
- 循环肿瘤DNA(ctDNA)检测产品:用于肿瘤早期筛查、疗效监测和复发预警的液体活检产品,部分在审查中被赋予优先地位,体现了对微创、动态监测技术的前瞻性支持。
- 传染病病原体检测:
- 在新冠肺炎疫情期间,多家企业的新冠病毒核酸检测试剂盒及变异株鉴别检测试剂通过应急特别审批程序迅速上市,保障了公共卫生应急需求。
- 针对耐药菌感染、呼吸道多病原体联合检测的分子诊断产品也因其重要的临床意义,部分进入了优先审批序列。
- 遗传病与罕见病诊断:
- 针对遗传性肿瘤综合征、遗传代谢病等的基因检测试剂盒,由于能助力罕见病早诊早治,也开始出现在优先审批的名单中,体现了政策对民生关切领域的倾斜。
三、技术趋势与行业影响
从获批或进入快速通道的产品来看,技术创新是核心驱动力。NGS技术、数字PCR、 CRISPR等前沿检测技术的应用日益广泛,产品正朝着“多(多靶标)、快(快速便捷)、准(高灵敏特异)、用(临床效用明确)”的方向发展。优先审批程序不仅加快了产品上市速度,也引导企业更加注重产品的临床验证和真实世界数据积累,促进了行业的高质量发展。
四、未来展望
随着《医疗器械监督管理条例》的深入实施以及审评审批制度改革的持续推进,预计将有更多具有原创性和临床急需的基因检测IVD产品通过特别或优先审批渠道惠及患者。监管科学的发展也将进一步优化审批标准与流程,在鼓励创新与确保安全有效之间实现更好平衡,持续推动我国基因检测产业创新生态的完善,为健康中国建设提供坚实的技术支撑。
(注:本文由火石研究院基于公开信息分析梳理,具体产品审批状态以国家药品监督管理局官方发布为准。)
最新产品